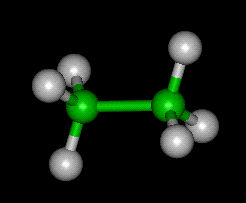
Zobrazit Ethqne Molekuly v 3D —>>ve 3D s Jsmol
Chemické a Fyzikální Vlastnosti Ethanu
Ethan je chemická sloučenina s chemickým vzorcem C2H6, strukturní vzorec CH3-CH3.
jedná se o Alkan, tedy alifatický uhlovodík. Při běžném tlaku a teplotě Ethan je bezbarvý, bez zápachu plyn; bod varu je ?88,6°; teplota tání je ?183.3°.
jedná se o nejjednodušší uhlovodík obsahující více než jeden atom uhlíku., Ethan je prominentní sloučenina průmyslového významu, přeměnou na ethylen nebo jeho použitím jako stavební blok pro petrochemický průmysl, pro syntézu polyethylenového plastu i jiných malých sloučenin.
Ethan byl poprvé synteticky vytvořen v roce 1834 Michaelem Faradayem a aplikoval elektrolýzu roztoku octanu draselného. Spletl si uhlovodíkový produkt této reakce s metanem a dále ho nezkoumal., Během období 1847-1849, ve snaze, aby chránily radikální teorie organické chemie, Hermann Kolbe a Edward Frankland produkoval ethan o snížení propionitril (ethyl kyanid) a ethyl-jodid draslíku, kov, a, stejně jako Faraday, elektrolýzou vodných acetáty. Oni však zaměnili produkt těchto reakcí za methylový radikál, spíše než dimer methylu, ethanu. Tato chyba byla opravena v roce 1864 Carlem Schorlemmerem, který ukázal, že produkt všech těchto reakcí byl ve skutečnosti Ethan.,
hlavní použití ethanu je v chemickém průmyslu při výrobě ethenu (ethylenu) krakováním parou. Po zředění párou a krátkém zahřátí na velmi vysoké teploty (900 °C nebo více) se těžké uhlovodíky rozpadají na lehčí uhlovodíky a nasycené uhlovodíky se stávají nenasycenými., Ethan je oblíbené pro ethene výroby, protože parní krakování ethanu je poměrně selektivní pro ethene, zatímco parní krakování těžších uhlovodíků výnosy produktu směs chudší na ethene, a bohatší na těžší alkenů (olefinů), jako propen (propylen) a butadienu, a v aromatických uhlovodíků.
Ethan se vyskytuje jako stopový plyn v zemské atmosféře, který má v současné době koncentraci na hladině moře 0.,5 ppbv, ačkoli jeho předindustriální koncentrace bude pravděpodobně nižší, protože významná část ethanu v dnešní atmosféře mohla vzniknout jako fosilní paliva. Ačkoli Ethan je skleníkový plyn, je mnohem méně hojný než metan a také méně účinný ve vztahu k hmotnosti. Byl také detekován jako stopová složka v atmosféře všech čtyř obřích planet a v atmosféře Saturnova měsíce Titan.
Viz také:
jaká je geometrie molekuly metanu? Interaktivní činnost, která zahrnuje jsmol applet metanu.















