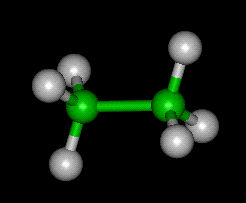
Om de Ethqne Molecuul in 3D – – – – >>in 3D met Jsmol
Chemische en Fysische Eigenschappen van Ethaan
Ethaan is een chemische stof met de chemische formule C2H6, structuurformule CH3-CH3.
Het is een alkaan, dat wil zeggen een alifatische koolwaterstof. Bij normale druk en temperatuur is ethaan een kleurloos, reukloos gas; kookpunt is ?88,6°; smeltpunt is ?183.3°.
Het is de eenvoudigste koolwaterstof die meer dan één koolstofatoom bevat., Ethaan is een prominente verbinding van industrieel belang, door het om te zetten in ethyleen of te gebruiken als bouwsteen voor de petrochemische industrie, voor de synthese van polyethyleen plastic en andere kleine verbindingen. ethaan werd voor het eerst synthetisch gemaakt in 1834 door Michael Faraday, waarbij elektrolyse van een kaliumacetaatoplossing werd toegepast. Hij zag het koolwaterstofproduct van deze reactie aan voor methaan en onderzocht het niet verder., In de periode 1847-1849 produceerden Hermann Kolbe en Edward Frankland ethaan door de reductie van propionitril (ethylcyanide) en ethyljodide met kaliummetaal en, net als Faraday, door de elektrolyse van waterige acetaten. Zij, echter, verwarden het product van deze reacties voor methylradicaal, eerder dan het dimeer van methyl, ethaan. Deze fout werd in 1864 gecorrigeerd door Carl Schorlemmer, die aantoonde dat het product van al deze reacties in feite ethaan was.,
ethaan wordt voornamelijk gebruikt in de chemische industrie bij de productie van etheen (ethyleen) door stoomkraken. Bij verdunning met stoom en kort verhit tot zeer hoge temperaturen (900 °C of meer) breken zware koolwaterstoffen af in lichtere koolwaterstoffen en worden verzadigde koolwaterstoffen onverzadigd., Ethaan wordt begunstigd voor de productie van etheen omdat het stoomkraken van ethaan vrij selectief is voor etheen, terwijl het stoomkraken van zwaardere koolwaterstoffen een productmengsel oplevert dat armer is aan etheen en rijker is aan zwaardere alkenen (olefinen) zoals propeen (propyleen) en butadieen, en aan aromatische koolwaterstoffen.
ethaan komt voor als een spoorgas in de atmosfeer van de aarde, met momenteel een concentratie op zeeniveau van 0.,5 ppbv, hoewel de pre-industriële concentratie waarschijnlijk lager is geweest, aangezien een aanzienlijk deel van het ethaan in de huidige atmosfeer als fossiele brandstoffen kan zijn ontstaan. Hoewel ethaan een broeikasgas is, is het veel minder overvloedig dan methaan en ook minder efficiënt ten opzichte van massa. Het is ook gedetecteerd als een spoorcomponent in de atmosferen van alle vier de reuzenplaneten, en in de atmosfeer van Saturnus ‘ maan Titan.
zie ook:
Wat is de geometrie van het methaanmolecuul? Een interactieve activiteit die de jsmol applet van methaan omvat.















