fenolftaleïne chemische eigenschappen, Gebruik, productie
zuur–base indicator
fenolftaleïne is een ander zwak organisch zuur. Het is niet bijzonder wateroplosbaar, dus lossen we het over het algemeen op in waterige ethanol. De ethanol verklaart de aangename, zoete geur van fenolftaleïne oplossingen.
fenolftaleïne is kleurloos en helder in zure oplossingen, maar geeft een intense puce roze kleur in alkalische oplossingen met een hogere pH, met λ(max) = 552 nm., De gekleurde vorm van fenolftaleïne bevat een chinongedeelte; in feite heeft elke chromofoor op basis van een Chinon een rode kleur. Maar als een oplossing wordt bereid bij pH 7 (bijvoorbeeld zoals bepaald met een pH-meter), vinden we dat de fenolftaleïne-indicator nog kleurloos is, en de roze kleur verschijnt pas wanneer de pH 8,2 bereikt. Daarom hebben we een probleem: de indicator heeft geen neutraliteit gedetecteerd, omdat hij bij een te hoge pH-waarde van kleur verandert. in feite is slechts een kleine stapsgewijze toevoeging van alkalioplossing nodig om de pH-waarde van de oplossing aanzienlijk te verhogen met meerdere pH-eenheden., Met andere woorden, een fractie van een druppel alkali-oplossing is het enige verschil tussen pH 7 (bij het ware volume bij neutralisatie) en pH 8 wanneer het fenolftaleïne verandert van kleurloos naar puce roze.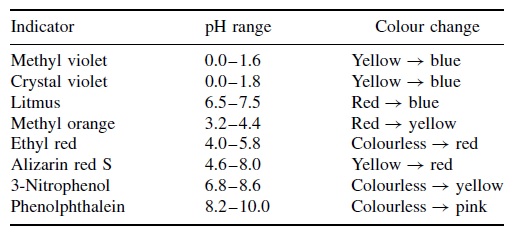
figuur 1 geeft de pH-veranderingen voor een reeks gemeenschappelijke pH-indicatoren weer. De kleur verandert over een breed scala aan ph ‘ s, de exacte waarde afhankelijk van de gekozen indicator. Methylviolet verandert van geel naar blauw als de pH tussen 0 en 1,6 toeneemt. Aan het tegenovergestelde uiterste reageert fenolftaleïne op pH-veranderingen in het bereik van 8,2 tot 10.,
chemische eigenschappen
fenolftaleïne is een zwak organisch zuur dat bij kamertemperatuur voorkomt als witte of microstripgele kleine kristallen, reukloos, smaakloos, onoplosbaar in water en oplosbaar in alcohol (ethanol) en ether. Wanneer opgelost in alcoholoplossing, kan het worden gemaakt van zuur en alkali-indicator. Het is kleurloos in zure oplossing terwijl het tentoonstellen van rode kleur in de carbonaatoplossing van alkalimetaal. Echter, indien geplaatst in de geconcentreerde alkali-oplossing, zal het kleurloos Tri-metaalzout produceren, zodat de rode kleur zal vervagen., Gezien deze eigenschap, gebruikt het laboratorium het algemeen als een soort zuur en alkali titratieindicator met de verkleuringswaaier van PH die rond 8.2 aan 10.0 zijn, die van kleurloos aan rood draaien. Wanneer het fenolftalein-reagens in water of neutrale, zure waterige oplossing wordt gedropt, zal er witte troebelheid zijn. Dit is te wijten aan dat de alcohol gemakkelijk oplosbaar is in water, zodat het reagens in water onoplosbare fenolftaleïne wordt neergeslagen., De andere belangrijke toepassingen zijn:
1, de farmaceutische grondstoffen in de farmaceutische industrie: het is geschikt voor gewone hardnekkige constipatie, waaronder tabletten, zetpillen en andere formuleringen.
2, kan het worden gebruikt voor organische synthese: voornamelijk gebruikt in de synthese van kunststoffen, met name in de synthese van de ftalazinon poly arylether keton poly arylether keton polymeren., Dit soort polymeren, vanwege de uitstekende hittebestendigheid, waterbestendigheid, corrosiebestendigheid, hitteveroudering weerstand en goede verwerkbaarheid, vezels, coatings en composieten gemaakt van het worden veel gebruikt op het gebied van elektrische en elektronische apparatuur, vervoer en ruimtevaart, atoomenergietechniek en militair.
3, gebruikt als zuur-en alkali-indicator, titratie-indicator voor niet-waterige oplossingen en analysereagentia voor chromatografie.,
algemene beschrijving
fenolftaleïne werkt voornamelijk in op de dikke darm, die in 4 tot 8 uur semi-vloeibare excreta produceert met weinig of geen koliek. De bewering dat gele fenolftaleïne drie keer sterker is dan wit blijft onbewezen. Als gevolg van de enterohepatische circulatie is het effect van een enkele dosis houdbaar gedurende 3 tot 4 dagen. Het medicijn is een actief lid van veel laxeermiddelen die legaal zonder voorschrift kunnen worden verkocht.ernstige bijwerkingen komen zelden voor, maar kunnen optreden bij overmatig gebruik., Fenolftaleïne moet worden vermeden bij ouderen, omdat de langdurige rol ervan ernstige uitputting van water en elektrolyten kan veroorzaken. Dermatitis (vaste uitslag, jeuk, branderig gevoel, blaarvorming en resterende pigmentatie) kan optreden bij allergische patiënten. Er waren meldingen van een fatale anafylaxie, maar er was geen duidelijk oorzakelijk verband met fenolftaleïne. Er zijn af en toe meldingen van niet-trombocytopenische purpura. Langdurige toediening kan soms veroorzaakt uitdroging en elektrolyt onbalans als gevolg van overmatige diarree. Fenolftaleïne veroorzaakt alkalische urine of feces roze.,
fenolftaleïne moleculaire structuur
dit product kan worden verkregen door het mengen van ftaalzuuranhydride met fenol, gevolgd door co-verhitting met zwavelzuur.fenolftaleïne heeft de chemische naam 2-benzoëzuur. Molecuulformule: C20H16O4, relatieve molecuulmassa: 318.33. De structuurformule is weergegeven in Figuur 1 (in feite bestaat het vaak in de vorm van kleurloos lacton, zie Figuur 2). Het verschijnt als triclinisch wit tot geelachtig kristallijn poeder met het smeltpunt van 237 ~ 259 ℃ en de relatieve dichtheid van 1,277 (20/4 ℃)., Het is gemakkelijk oplosbaar in ethanol, ether en andere organische oplosmiddelen, lichtjes oplosbaar in water. Het heeft een zwakke zuurgraad en wordt bijna volledig gepresenteerd in de molecuultoestand, zelfs in zeer verdunde oplossing. Het is oplosbaar in alkalische oplossing, die rode kleur in alkalische oplossing tentoonstellen, maar is kleurloos in zure oplossing. De drie benzeenringen in het fenolftaleinmolecuul zijn verbonden met de koolstofatomen van een SP3 hybride centrum, en er is geen geconjugeerde relatie tussen de benzeenringen, die kleurloos zijn., Na het tegenkomen van alkali, de lacton ring open en genereren dinatriumzout, de centrale koolstofatomen worden overgebracht naar de SP2 hybride staat, met benzoquinon structuur. Op dit moment, vormt het geconjugeerd systeem met de drie benzeenringen die rood zijn; maar boven alkali, maar het wordt verder omgezet in SP3 hybride staat zodat het geconjugeerde systeem verdwijnt, zal de kleur ook wijken.
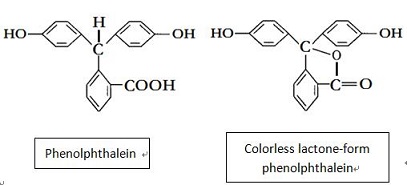
Fenolftalein-indicator
Fenolftalein-indicator is een veelgebruikte zuur/alkali-titratie-indicator in de Analytische Chemie., Fenolftaleïne, in alkalische oplossing, heeft zijn kleurloze lactonring open om quinonstructuur te vormen met de kleur die rood vertoont. Bij het komen over sterke alkali, kan phenolphthalein in kleurloze carboxylate worden omgezet. Het kleurbereik is pH 7.0 (kleurloos) ~ 10.0 (rood). De testoplossing werd bereid door 1 g 90% ethanol per liter ethanol op te lossen.
fenolftaleïne is kleurloos in een oplossing met een pH lager dan 8,5 en wordt rood bij een pH hoger dan 9., Bij overmatige hoeveelheid alkali en geen kleur verloopt het kleurproces als volgt: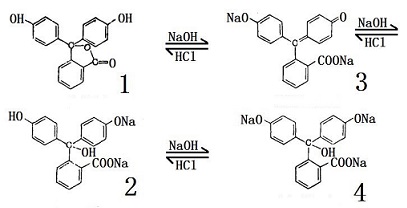 fenolftaleïne wordt, indien gebruikt als zuur-alkali titratie-indicator, over het algemeen gebruikt bij een concentratie van 1%. 1 g fenolftaleïne werd opgelost in 100 ml 80% alcohol; laat langzaam 0,1 mol / l natriumhydroxide roodachtig vallen (voor het neutraliseren van de kleine hoeveelheid zuur die mogelijk in alcohol aanwezig is). Het pH-bereik van verkleuring is 8,2 tot 10. Het is kleurloos bij PH <8.2, is rood bij pH> 10., Het principe van kleurverandering is voornamelijk te wijten aan dat onder verschillende zuur-en alkaliomstandigheden, de structuur van het molecuul zelf verandert en verder veroorzaakt verschillende kleuren. Het mengen van de fenolftaleïne en andere indicatoren kan de veel gebruikte indicator formuleren (ook bekend als een algemene indicator).meng 1,3 gram fenolftaleïne, 0,9 gram broomthymolblauw, 0,4 gram methylrood en 0,2 gram thymolblauw en los op in 1 liter 70% tot 80% alcohol. Na het volledig oplossen, voeg dan wat 0,1 mol / l natriumhydroxide toe waardoor het net groen wordt voor het aanbrengen., Het voordeel is dat de kleurverandering met de pH-veranderingen opmerkelijk is: rood voor pH = 4; oranje voor pH 5; Geel voor pH 6, Groen voor pH 7; cyaan voor pH 8; blauw voor pH 9; en paars voor pH 10.indien nodig kunnen verschillende algemene indicatoren worden geformuleerd. Fenolftaleïne indicator wordt niet alleen gebruikt in laboratoria, maar ook op grote schaal gebruikt in de industriële en agrarische productie., Naast het feit dat het wordt gebruikt in de pH-regeling van de reactie-en zuur/alkalitratieanalyse tijdens de productie van chemische producten, wordt het ook gebruikt voor het bepalen van de pH van het weven in de druk-en verfindustrie. Dit is erg belangrijk voor druk-en verfverwerking. Bijvoorbeeld, als de gemerceriseerde doek resterende alkali bevat die niet is gewassen, zal het verven geen glans hebben. De fenolftaleïne-indicator alleen kan echter alleen bepalen of de textuur van het weefsel zuur of alkalisch is en zijn pH-bereik, en kan de specifieke pH niet verder bepalen., Het brede scala van indicatoren hierboven gebruikt kan duidelijk worden weerspiegeld van de zuur – en alkalisterkte in de doek. Fenolftaleïne, in de geneeskunde kan ook worden gebruikt als laxeermiddel, omdat het de peristaltiek van de darm kan stimuleren om ontlasting te bevorderen. Nochtans, kan het soms allergische reacties zoals dermatitis veroorzaken, dus moet met aandacht worden gebruikt.
fenolftaleïne wordt, indien gebruikt als zuur-alkali titratie-indicator, over het algemeen gebruikt bij een concentratie van 1%. 1 g fenolftaleïne werd opgelost in 100 ml 80% alcohol; laat langzaam 0,1 mol / l natriumhydroxide roodachtig vallen (voor het neutraliseren van de kleine hoeveelheid zuur die mogelijk in alcohol aanwezig is). Het pH-bereik van verkleuring is 8,2 tot 10. Het is kleurloos bij PH <8.2, is rood bij pH> 10., Het principe van kleurverandering is voornamelijk te wijten aan dat onder verschillende zuur-en alkaliomstandigheden, de structuur van het molecuul zelf verandert en verder veroorzaakt verschillende kleuren. Het mengen van de fenolftaleïne en andere indicatoren kan de veel gebruikte indicator formuleren (ook bekend als een algemene indicator).meng 1,3 gram fenolftaleïne, 0,9 gram broomthymolblauw, 0,4 gram methylrood en 0,2 gram thymolblauw en los op in 1 liter 70% tot 80% alcohol. Na het volledig oplossen, voeg dan wat 0,1 mol / l natriumhydroxide toe waardoor het net groen wordt voor het aanbrengen., Het voordeel is dat de kleurverandering met de pH-veranderingen opmerkelijk is: rood voor pH = 4; oranje voor pH 5; Geel voor pH 6, Groen voor pH 7; cyaan voor pH 8; blauw voor pH 9; en paars voor pH 10.indien nodig kunnen verschillende algemene indicatoren worden geformuleerd. Fenolftaleïne indicator wordt niet alleen gebruikt in laboratoria, maar ook op grote schaal gebruikt in de industriële en agrarische productie., Naast het feit dat het wordt gebruikt in de pH-regeling van de reactie-en zuur/alkalitratieanalyse tijdens de productie van chemische producten, wordt het ook gebruikt voor het bepalen van de pH van het weven in de druk-en verfindustrie. Dit is erg belangrijk voor druk-en verfverwerking. Bijvoorbeeld, als de gemerceriseerde doek resterende alkali bevat die niet is gewassen, zal het verven geen glans hebben. De fenolftaleïne-indicator alleen kan echter alleen bepalen of de textuur van het weefsel zuur of alkalisch is en zijn pH-bereik, en kan de specifieke pH niet verder bepalen., Het brede scala van indicatoren hierboven gebruikt kan duidelijk worden weerspiegeld van de zuur – en alkalisterkte in de doek. Fenolftaleïne, in de geneeskunde kan ook worden gebruikt als laxeermiddel, omdat het de peristaltiek van de darm kan stimuleren om ontlasting te bevorderen. Nochtans, kan het soms allergische reacties zoals dermatitis veroorzaken, dus moet met aandacht worden gebruikt.
fenolftaleïne-testpapier
fenolftaleïne-testpapier is een van de eenvoudige testdocumenten die vaak worden gebruikt bij chemische analyse. Het is zeer gericht. Het wordt rood in het geval van alkali, en is kleurloos in zure en neutrale oplossing., Om de aanwezigheid van ammoniak in de lucht te testen, zal het lichtrood lijken. De bereidingsmethode is eenvoudig: het filtreerpapier wordt ondergedompeld in een fenolftaleïneoplossing en na volledige absorptie voor droging verwijderd.
Farmacologie en toxicologie
fenolftaleïne kan worden gebruikt voor de behandeling van gebruikelijke refractaire constipatie, die voornamelijk op het colon werkt. Na orale toediening kan het langzaam worden afgebroken onder het effect van de dunne darm alkalische vloeistof om oplosbaar natriumzout te vormen, waardoor de plexus in de darmwand wordt gestimuleerd., Het werkt direct in op de intestinale gladde spieren en verhoogt de peristaltiek, terwijl het ook de absorptie van water in de darm remt, zodat water en elektrolyt zich in de dikke darm ophoopt, wat resulteert in een laxerend effect. Het heeft een mild effect en veroorzaakt zelden darmkrampen.
farmacokinetiek
na orale toediening wordt ongeveer 15% geabsorbeerd., De geabsorbeerde geneesmiddelen bestaan voornamelijk in de vorm van glucuronide dat uit urine of de ontlasting moet worden uitgescheiden, wat kan ook worden uitgescheiden in de darm via de gal, opnieuw geabsorbeerd in de darm, om darm – levercirculatie te vormen en de roltijd te verlengen. 4 tot 8 uur na de toediening van het geneesmiddel, zullen de patiënten zachte ontlasting ontladen. De uitscheidingstijd voor toediening van het geneesmiddel eenmaal heeft 3 tot 4 dagen nodig. Dit product kan ook uit melk worden uitgescheiden.,
bijwerkingen
fenolftaleïne heeft voornamelijk effect in de dikke darm, wat leidt tot de vorming van een kleine hoeveelheid semi-vloeibare feces in 4 tot 8 uur zonder koliek. De bewering dat de gele fenolftaleïne driemaal sterker is dan de witte versie is niet bewezen. Als gevolg van de enterohepatische circulatie kan het effect van een enkele dosis 3 tot 4 dagen duren. Dit medicijn is een actief lid in veel laxeermiddelen die legaal kunnen worden verkocht zonder voorschrift van een arts.ernstige bijwerkingen komen zelden voor, maar kunnen vaker voorkomen., Voor ouderen moet fenolftaleïne worden opgehangen, omdat het blijvende effect ervan ernstige uitputting van water en elektrolyten kan veroorzaken. Bij allergische patiënten, kan het veroorzaken optreden dermatitis (vaste uitslag, jeuk, brandend gevoel, blaarvorming, en resterende pigmentatie). Er zijn meldingen van fatale allergische reacties, maar er is nog geen verband vastgesteld met fenolftaleïne. Er zijn af en toe meldingen van niet-trombocytopenische purpura en het optreden van uitdroging en elektrolytenonbalans veroorzaakt overmatige diarree na langdurige toepassing., Fenolftaleïne maakt alkalische urine of uitwerpselen roze.
toepassing
dit product is een veelgebruikte zuurindicator met een kleurverandering tussen pH 8,2 (kleurloos) en 10,0 (rood). Fenolftaleïne is ook een medicijn, kan worden gebruikt als een laxeermiddel, dat op de dikke darm werkt voor de behandeling van constipatie.
gebruikt als zuur-base-indicator; als irriterend laxeermiddel voor de behandeling van constipatie
productiemethode
wordt het afgeleid van de condensatie van ftaalzuuranhydride en fenol.,
chemische eigenschappen
wit tot lichtgeel kristalpoeder
gebruik
anthelmintisch
gebruik
gebruikt als indicator voor zuurmetrische titraties.
definitie
een zuur-base-indicator die colorlessin zure oplossingen is en rood wordt als de pH boven het transitiebereik van8–9,6 uitstijgt. Het wordt gebruikt als indicator in titratieswaarvoor het eindpunt duidelijk aan de basiszijde ligt (pH>7), bijvoorbeeld oxaalzuur of kaliumwaterstofartraat tegen bijtende soda.
definitie
fenolftaleïne: een kleurstof die wordt gebruikt als indicator voor anacid-base., Het is kleurloos onder pH 8 en Rood Boven pH 9,6. Het wordt gebruikt in titraties die weakacids en sterke basissen impliceren. Het wordt ook gebruikt als laxeermiddel.,Bold laxine;Bom-bon;Bon-bon;Canisan;Certolax;D & m tablets;Darmol;Euchessinia;Evac-qwik tablets;Evactil;Feen-a-mint;Fractines vichy;Fractine-vichy;Fructines-vichy;Kalimalterin;Kest;Kondremul with phenolphtalein;Laxante yer;Laxatabs;Laxatone;Laxen busto;Minilax;Modane plus;Mucinum;Musilaks;Neoprunex;Neopurghes;Novopuren;Paradeines;Peplax;Petrolaglar emulsion;Petro-mul-phen;Phillips laxcaps;Prifunal;Prunetta;Pugrante el aleman;Purganol;Purganos-daguin;Purgant aleman;Purgante orravan;Purgenum;Purgestol;Purgoids;Purgyl;Purjen sahap;Sarolax;Thalinol mrt;Unisvelt;Veracolate.,
World Health Organization (WHO)
fenolftaleïne wordt op grote schaal gebruikt als laxeermiddel sinds de ziekte in 1902 voor het eerst werd beschreven. Omdat het enterohepatischecirculatie ondergaat, wordt het langzaam geëlimineerd en is het in verband gebracht met bijwerkingen,met name huidreacties, kaliumverlies en atonie. Dit heeft ertoe geleid dat fenolftaleïne in verschillende landen uit farmaceutische preparaten is gehaald.Elders blijft het beschikbaar, vaak in over-the-counter voorbereidingen.
veiligheidsprofiel
bevestigd carcinogeen., Us Food and Drug Administration adviseert verwijdering van laxerende formuleringen. Matig toxisch via intraperitoneale route. Systemische effecten bij de mens: veranderingen in de samenstelling van de urine, gastritis, misselijkheid of braken. Gebruikt in de geneeskunde als laxeermiddel; in de chemie als indicator. Bij verhitting tot ontbinding stoot het acrid rook uit en irriterende dampen
carcinogeniteit
fenolftaleïne wordt redelijkerwijs geacht een carcinogeen voor de mens te zijn op basis van voldoende aanwijzingen voor carcinogeniteit uit studies bij proefdieren.,
zuiveringsmethoden
lossen het op in EtOH (7 ml / g), verdunnen het vervolgens met acht volumes koud water, filteren en verwarmen op een waterbad om het grootste deel van de alcohol en het fenolftaleïne dat neerslaat, te verwijderen en te drogen in vacuüm.















