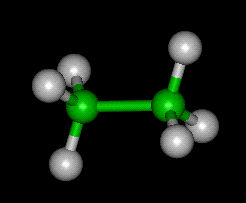
Para Visualizar o Ethqne Molécula em 3D —>>em 3D com Jsmol
Propriedades Físicas e Químicas do Etano
Etano é um composto químico com fórmula química C2H6), fórmula estrutural CH3-CH3. é um alquano, isto é, um hidrocarboneto alifático. A pressão e temperatura normais de etano é um gás incolor e inodoro; ponto de ebulição é ?88,6°; ponto de fusão é ?183.3°.
é o hidrocarboneto mais simples contendo mais de um átomo de carbono., Etano é um composto proeminente de importância industrial, convertendo-o em etileno ou usando-o como um bloco de construção para a indústria petroquímica, para a síntese tanto de plástico polietileno e outros pequenos compostos.
etano foi inicialmente criado sinteticamente em 1834 por Michael Faraday, aplicando eletrólise de uma solução de acetato de potássio. Ele confundiu o produto hidrocarboneto desta reação com metano, e não investigou mais., Durante o período de 1847-1849, em um esforço para justificar a teoria radical da química orgânica, Hermann Kolbe e Edward Frankland produzido etano pelas reduções de propionitrile (etil cianeto) e etílico iodeto de potássio, de metal, e, como fez Faraday, por eletrólise aquosa de acetatos. Eles, no entanto, confundiram o produto dessas reações com RADical de metila, ao invés do dímero de metil, etano. Este erro foi corrigido em 1864 por Carl Schorlemmer, que mostrou que o produto de todas essas reações era de fato ethane., a principal utilização do etano é na indústria química na produção de eteno (etileno) por craqueamento a vapor. Quando diluídos com vapor e brevemente aquecidos a temperaturas muito elevadas (900 °C ou mais), os hidrocarbonetos pesados decompõem-se em hidrocarbonetos mais leves e os hidrocarbonetos saturados tornam-se insaturados., Etano é favorecido para a produção de eteno porque o craqueamento a vapor de etano é bastante seletivo para o eteno, enquanto o craqueamento a vapor de hidrocarbonetos mais pesados produz uma mistura de produtos mais pobre em eteno, e mais rico em alcenos mais pesados (olefinas), como propeno (propileno) e butadieno, e em hidrocarbonetos aromáticos.
etano ocorre como um gás residual na atmosfera terrestre, tendo atualmente uma concentração no nível do mar de 0.,5 ppbv, embora sua concentração pré-Industrial provavelmente tenha sido menor, uma vez que uma proporção significativa do etano na atmosfera de hoje pode ter se originado como combustíveis fósseis. Embora o etano seja um gás de efeito estufa, é muito menos abundante do que o metano e também menos eficiente em relação à massa. Ele também foi detectado como um componente traço nas atmosferas de todos os quatro planetas gigantes, e na atmosfera da lua de Saturno Titã.
Ver também:
Qual é a geometria da molécula de metano? Uma actividade interactiva que inclui a applet jsmol do metano.















