polimerização: como os polímeros são feitos
a junção de uma longa cadeia de moléculas é conhecida como polimerização.
para manter as coisas simples, vamos olhar para um tipo de polimerização chamado “polimerização de adição”. Além disso, a polimerização—você adivinhou—os monômeros são simplesmente adicionados em um padrão repetitivo. Isto não resulta na criação de qualquer outra substância adicional.
(a outra forma pela qual os polímeros podem ser criados é denominada polimerização de condensação., Neste processo, quando cada monômero é adicionado à cadeia, uma molécula adicional, pequena—como a água—é criada como um subproduto. Nylon e poliéster são feitos assim.)
A polimerização da adição baseia-se num monómero com uma ligação dupla que liga dois átomos de carbono. Uma molécula chamada de radical livre é introduzida, o que faz com que a dupla ligação se abra e se conecte com a próxima molécula de monômero. A cadeia polimérica forma-se quando a mesma unidade básica é repetida vezes sem conta numa estrutura de cadeia regular., Embora usar radicais livres desta forma não seja uma ideia nova, os químicos estão descobrindo regularmente moléculas que são muito mais eficientes em fazer polímeros. Isto significa que os polímeros podem ser feitos mais rápido, mais barato, mais limpo e com maior controle do produto final.
vamos ampliar e olhar para este processo em um pouco mais de detalhe, usando a formação de polietileno como um exemplo. o polietileno é o polímero sintético mais simples. É feito de apenas um tipo de monômero-etileno, que é feito de dois átomos de carbono e dois átomos de hidrogênio., (Outros polímeros podem ser constituídos por dois ou mais monómeros diferentes. O polietileno é formado quando muitos milhares de moléculas de etileno são unidas de ponta a ponta.
o processo inicia-se com o aquecimento de uma molécula, como o peróxido de hidrogénio.
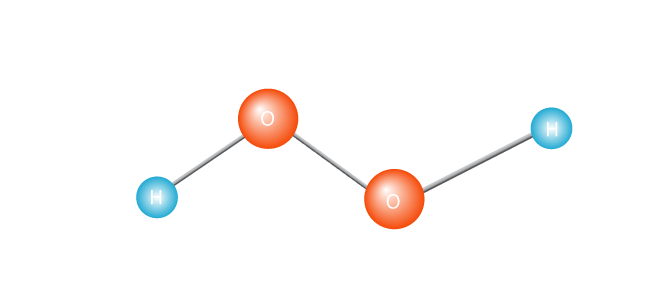
isto faz com que se quebre em dois, criando um radical livre. Um radical livre é uma molécula com um único elétron não emparelhado. Os elétrons são os extrovertidos do mundo atômico; eles realmente não lidam com estar sozinhos., Ou, para ser técnico, uma molécula com um electrão não emparelhado na sua concha externa de Valência é uma molécula instável. De qualquer forma, o elétron solitário vai querer fazer par com outro elétron.
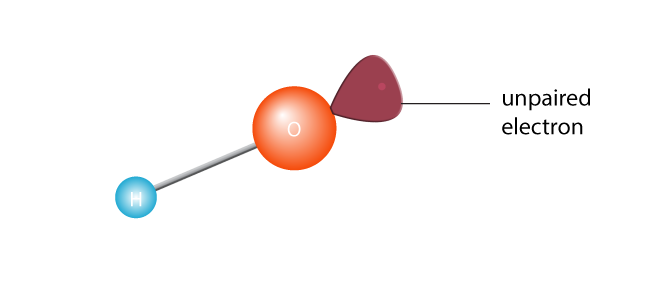
agora introduzimos a nossa molécula de etileno.
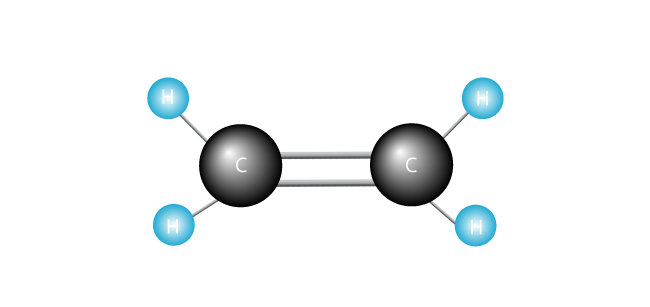
o radical livre procura por outro electrão com o qual parará o seu único electrão solitário.,
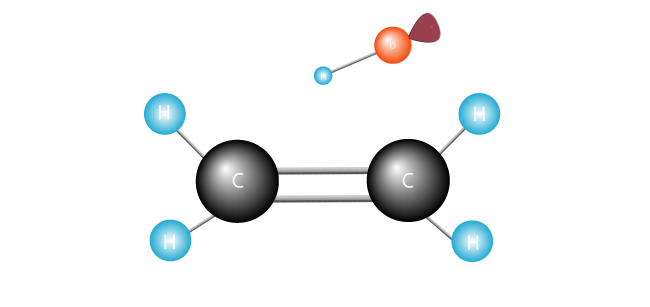
ataca a dupla ligação que une os dois carbonos na molécula de etileno e atravessa um electrão.
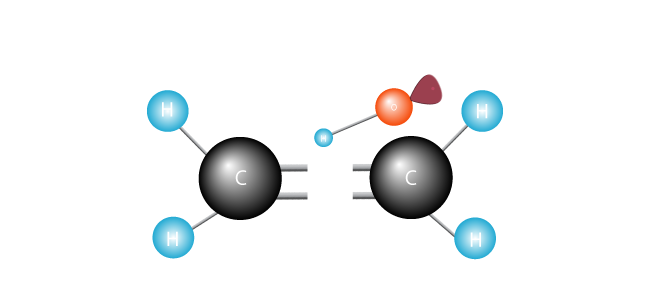
seus elétrons emparelhados alegremente, o radical livre junta-se a um dos Carbões.
o outro carbono, anteriormente emparelhado felizmente, agora tem um elétron não emparelhado. Tornou-se um radical livre, com um elétron não emparelhado ansioso para se juntar com outro para fazer um par.,
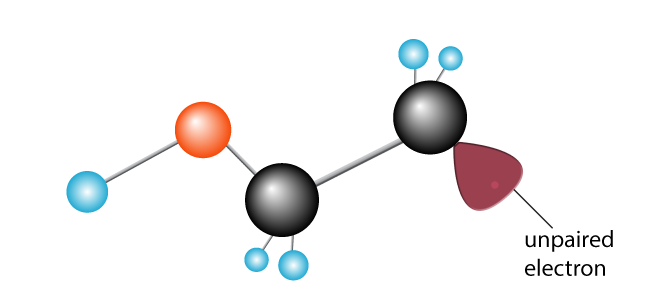
é introduzida uma segunda molécula de etileno. O recém-criado radical livre quebra a ligação carbono-carbono, roubando um elétron, e criando um novo radical livre com um único elétron não emparelhado no final.
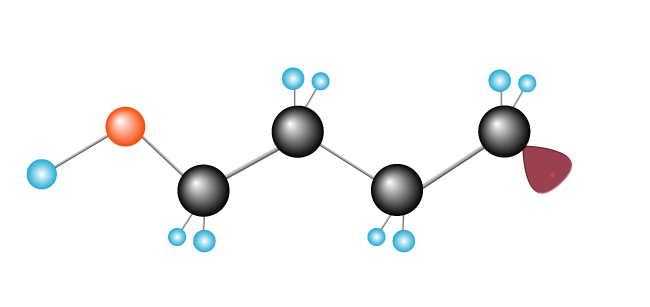
isto continua, como uma reacção em cadeia, com uma cadeia longa a formar-se à medida que mais moléculas de etileno são adicionadas.,
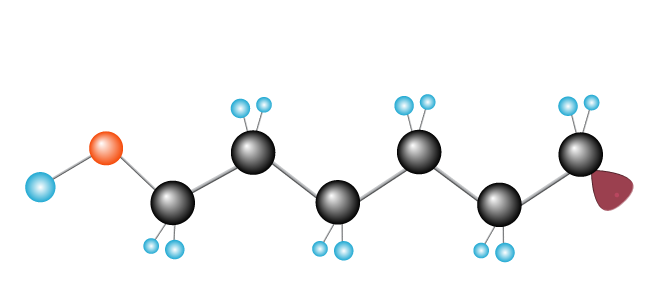
O processo continua até que os radicais livres atende a outro radical livre, completando a cadeia.
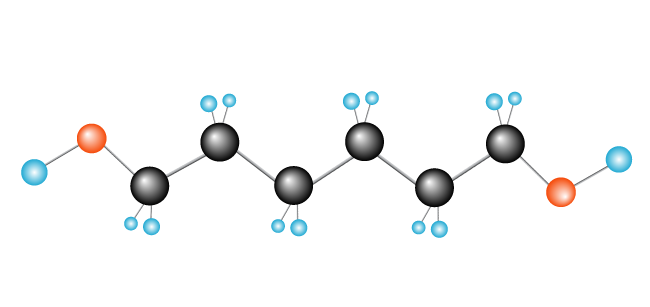
Agora temos o nosso polímero, polietileno, constituído pelo monómero (unidade repetitiva) etileno., outros exemplos de polímeros formados desta forma são o policloroetileno (PVC), utilizado para fazer coisas como canalizações e isolamento para cabos eléctricos, e polipropileno, utilizado em produtos como Patos De Borracha (e outros brinquedos) e, quando transformados em fibras, tapetes.















